Sinónimos: Anemia de Cooley
Anemia mediterránea
Prevalencia: Desconocido
Herencia: Autosómico recesivo
Edad de inicio o aparición: Neonatal / infancia
Resumen:
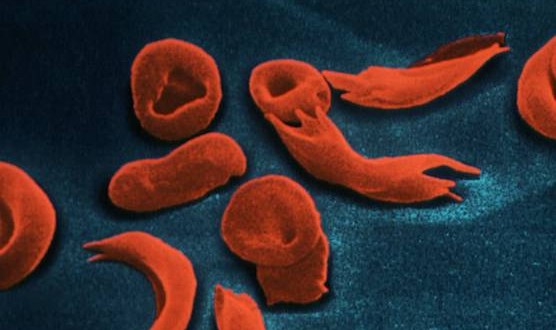
La beta-talasemia mayor (BTM) es una forma grave de talasemia por déficit de cadenas beta de globina y se caracteriza por una anemia intensa que requiere transfusiones periódicas de glóbulos rojos.
La incidencia anual de casos sintomáticos se estima en 1/100.000 en todo el mundo y 1/10.000 en la UE. La prevalencia de esta forma no se conoce.
Debuta en la infancia con: anemia muy intensa, palidez, ictericia y manifestaciones acompañantes como diarrea, irritabilidad, episodios febriles recurrentes y distensión abdominal progresiva debida a la hepatoesplenenomegalia, a veces masiva. Sin medicación vitamínica coadyuvante y tratamiento transfusional insuficiente estos pacientes muestran un importante retraso del crecimiento con escasa musculatura, úlceras maleolares y genu valgo. La excesiva regeneración eritropoyética puede dar lugar a masas tumorales por hematopoyesis extramedular, con deformidades de huesos largos y alteraciones craneofaciales muy características (prominencia frontal, eminencia malar prominente o depresión del puente nasal). En pacientes transfundidos regularmente, el desarrollo tiende a la normalidad, pero se suelen producir complicaciones debidas a la sobrecarga de hierro por efecto transfusional como es el retraso de la maduración sexual. Complicaciones más tardías ligadas a sobrecarga de hierro: miocardiopatía dilatada, arritmias, fibrosis hepática y cirrosis, diabetes mellitus e insuficiencia de paratiroides, tiroides, hipófisis y, con menor frecuencia, de glándulas suprarrenales.
La BTM obedece a mutaciones puntuales o, más raramente, a deleciones en el gen HBB (11p15.5), lo que lleva a la disminución (beta +) o ausencia (beta 0) de síntesis de las cadenas beta de la hemoglobina (Hb). Las mutaciones que causan BTM son homocigotas para un mismo alelo mutado o doble heterocigotas para dos alelos mutados diferentes.
Debe sospecharse este diagnóstico en niños menores de 2 años con anemia microcítica grave, palidez intensa, ictericia moderada y hepatoesplenomegalia. El análisis de sangre muestra una disminución de la concentración de Hb (<7g/dl), del volumen corpuscular medio (VCM) (50-70 fl), hemoglobina corpuscular media (HCM) (12-20 pg), anisopoiquilocitosis y presencia de eritroblastos en el frotis de sangre periférica. El estudio de Hb y el análisis genético molecular confirman el diagnóstico.
El diagnóstico diferencial incluye: anemia sideroblástica congénita, anemias diseritropoyéticas congénitas (CDA) y otras situaciones con niveles elevados de HbF, como la leucemia mielomonocítica juvenil, la aplasia de medula ósea o la eritroblastopenia hereditaria.
El diagnóstico prenatal es posible mediante amniocentesis, si los dos alelos causantes han sido identificados previamente.
La transmisión es autosómica recesiva. El consejo genético informa sobre el patrón de herencia a pacientes y parejas de riesgo. El diagnóstico genético preimplantacional puede realizarse en familias en las que las mutaciones han sido previamente identificadas.
El tratamiento consiste en transfusiones periódicas de por vida para corregir la anemia, suprimir la eritropoyesis e inhibir la absorción gastrointestinal de hierro que se produce en los pacientes no transfundidos. La quelación del hierro debe iniciarse tras 10-15 transfusiones o cuando los niveles de ferritina estén por encima de 1.000 ng/ml. El manejo clínico debe incluir el tratamiento de las complicaciones por sobrecarga de hierro. La esplenectomía puede aportar una cierta mejora. El trasplante de médula ósea es actualmente el único tratamiento curativo de la enfermedad aunque, recientemente y por primera vez, se ha tratado con éxito un paciente mediante terapia génica.
En general, los pacientes que no reciben transfusiones regulares y una terapia quelante del hierro fallecen antes de la 2ª o 3ª década, mientras que la supervivencia es mayor en los pacientes transfundidos y quelados con regularidad. Las complicaciones cardíacas siguen siendo la principal causa de muerte.
Revisores expertos:
- Pr Renzo GALANELLO
- Dr R ORIGA
Última actualización: Mayo 2011
Fuente: http://www.orpha.net/consor/cgi-bin/Disease_Search.php?lng=ES&data_id=19171&Disease_Disease_Search_diseaseGroup=Anemia-de-Cooley&Disease_Disease_Search_diseaseType=Pat&Enfermedade%28s%29/grupo%20de%20enfermedades=Beta-talasemia-mayor–Anemia-de-Cooley-&title=Beta-talasemia-mayor–Anemia-de-Cooley-&search=Disease_Search_Simple