Sinónimos: –
Prevalencia: 1-9 / 1 000 000
Herencia: Autosómico recesivo
Edad de inicio o aparición: Infancia / Neonatal
Resumen
El síndrome de Sjögren-Larsson (SSL) es una enfermedad neurocutánea debido a una anomalía innata del metabolismo de lípidos y caracterizada por una ictiosis congénita, un déficit intelectual y espasticidad.
La prevalencia se estima en 1/250.000 y es más elevada en Suecia debido a un efecto fundador.
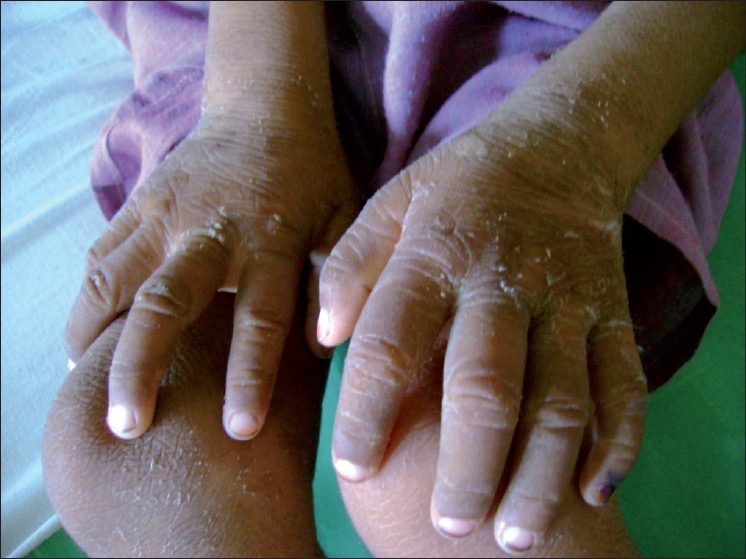
Los rasgos clínicos se desarrollan en el periodo prenatal y durante la infancia. En el nacimiento, suele darse una hiperqueratosis leve que evoluciona hacia una ictiosis generalizada, más desarrollada en las zonas de flexión, la nuca, el tronco y las extremidades. A diferencia de otras formas de ictiosis, el prurito es muy frecuente. También es frecuente en el momento del nacimiento una eritrodermia, que suele desaparecer con la edad. Los signos neurológicos aparecen durante el primer o segundo año de vida y se traducen en un retraso psicomotor, debido a una diplejia espástica, o, con mucha menor frecuencia, en una tetraplejia espástica. La mitad de los pacientes aproximadamente no son capaces de andar. Se producen convulsiones en un 40% de casos. El déficit intelectual varía de moderado a severo, aunque se han descrito unos pocos casos con inteligencia normal. Son frecuentes la disartria y un retraso en el habla. Suele darse una afectación oftalmológica, caracterizada por inclusiones cristalinas de la retina alrededor de la fóvea. Son frecuentes fotofobia y miopía. Se han descrito dermatoglifos anormales. Los pacientes suelen nacer prematuramente.
El SSL se debe a mutaciones del gen ALDH3A2 (17p11.2), que codifica para la aldehído graso deshidrogenasa (FALDH), una enzima necesaria en la oxidación de alcoholes grasos en ácidos grasos. Se han descrito más de 70 mutaciones, que incluyen sustituciones nucleotídicas, deleciones, inserciones y errores de splicing. La transmisión es autosómica recesiva. El síndrome se diagnostica midiendo la actividad de la FALDH o de la fatty alcohol oxidoreductase (FAO) en cultivos de fibroblastos obtenidos a partir de biopsias cutáneas.
El diagnóstico puede confirmarse por un cribado de las mutaciones conocidas con ayuda de una PCR alelo específica, o bien por secuenciación directa del gen ALDH3A2. En los niños no afectados aún de espasticidad, el diagnóstico diferencial incluye otras formas de ictiosis congénita, como la ictiosis lamelar o la eritrodermia congénita ictiosiforme (ver términos). Una vez aparecen los síntomas neurológicos, más tarde en la infancia, el diagnóstico diferencial incluye diversos síndromes neuro-ictiósicos, como la lipidosis con alteración del almacenamiento de triglicéridos (síndrome de Chanarin-Dorfman), la mucosulfatidosis y la enfermedad de Refsum (ver términos).
El diagnóstico prenatal es posible a partir de análisis bioquímicos o genéticos en amniocitos o en células de vellosidades coriónicas. El manejo implica la intervención de un equipo pluridisciplinar de neurólogos, dermatólogos, oftalmólogos, cirujanos ortopédicos y fisioterapeutas. El tratamiento de la ictiosis consiste en la aplicación tópica de queratolíticos o en la administración de retinoides sistémicos.
En general, las convulsiones responden favorablemente a los tratamientos antiepilépticos y la espasticidad es aliviada por intervenciones quirúrgicas. Una dieta especial con suplementos de ácidos grasos de cadena media puede mejorar la ictiosis, aunque sus efectos son moderados. Los pacientes suelen vivir hasta la edad adulta pero requieren cuidado de por vida. Los síntomas neurológicos y el déficit intelectual no evolucionan más tras la pubertad.
Los pacientes con síntomas tempranos suelen tener una afectación más grave.
Revisores expertos
- William RIZZO
Última actualización: Noviembre 2008
Fuente: Orphanet (Síndrome de Sjögren-Larsson)