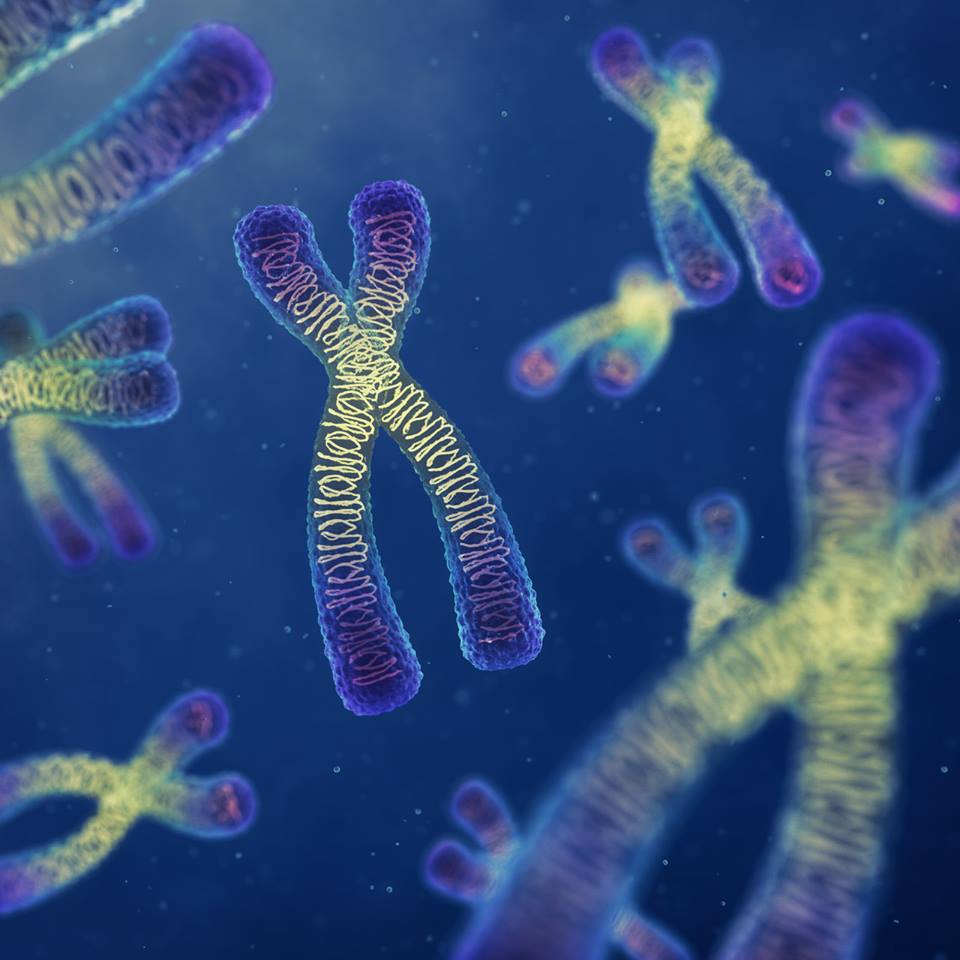
Una condición genética que típicamente afecta a los hombres más que a las mujeres, el síndrome de X frágil (FXS) es una enfermedad rara causada por daño al gen FMR1 ubicado en el cromosoma X, que a su vez no produce la proteína que normalmente produce. La enfermedad rara se caracteriza por una serie de déficits neurológicos, como convulsiones, junto con discapacidades del desarrollo, intelectuales y sociales.
Actualmente, no hay un tratamiento específico para la enfermedad; como tal, el manejo de la condición suele ser más de apoyo en lugar de curativo. Sin embargo, ahora, un nuevo ensayo clínico fundamental tiene como objetivo evaluar la seguridad y eficacia de un gel de cannabidiol (CBD) desarrollado por Zynerba Pharmaceuticals para tratar los comportamientos debilitantes asociados con la enfermedad.
El gel, denominado ZYN002, se evaluará en un ensayo multinacional aleatorizado, doble ciego, controlado con placebo, de 14 semanas en niños y adolescentes con FXS. A diferencia de la administración por vía oral, la administración transdérmica de ZYN002 permite que el fármaco se absorba a través de la piel al torrente sanguíneo y evita los posibles efectos adversos gastrointestinales asociados al evitar el tracto GI.
Aunque CBD, una sustancia derivada de la marihuana, enfrenta estrictas regulaciones de producción y fabricación, la aprobación de una solución oral de CBD para el síndrome de Lennox-Gastaut y el síndrome de Dravet por la Administración de Alimentos y Medicamentos (FDA) de EE. UU. Brinda esperanza para ZYN002.
«Estamos entusiasmados de iniciar CONNECT-FX, el primer estudio clínico de su clase que evalúa la administración transdérmica de ZYN002 como tratamiento para los comportamientos debilitantes asociados con el síndrome X frágil», dijo Armando Anido, presidente y director ejecutivo de Zynerba, en una declaración reciente. «Si tiene éxito, ZYN002 tiene el potencial de convertirse en el primer producto indicado para el tratamiento de los síntomas conductuales del síndrome de X frágil y ayudar a abordar las necesidades constantes de los niños y las familias afectadas por este síndrome».
El ensayo CONNECT-FX incluirá a aproximadamente 200 pacientes hombres y mujeres con FXS que tienen una mutación completa del gen FMR1 confirmado que abarca 20 sitios clínicos en los Estados Unidos, Australia y Nueva Zelanda. Para el estudio, los participantes serán aleatorizados 1: 1 para recibir ya sea el fármaco de investigación o el placebo. El género, el peso y la región geográfica del investigador determinarán la aleatorización.
El cambio desde el inicio hasta el final del período de tratamiento en la subescala de Evitación de Comportamiento Aberrante-Específico de la Comunidad FXS (ABC-CFXS) servirá como el punto final primario para la prueba. Los puntos finales secundarios del ensayo incluyen el cambio desde el inicio hasta el final del período de tratamiento en la puntuación de la subescala de Irritabilidad ABC-CFXS, la puntuación de la subescala Socialmente Insensible / Lethargic ABC-CFXS y la mejora en la Impresión Clínica Global (CGI-I) al final del período de tratamiento.
«En pacientes con X frágil, el aumento de la disponibilidad de cannabinoides endógenos tiene el potencial de impactar positivamente las conductas de evitación social y la ansiedad durante las interacciones sociales», agregó Elizabeth M. Berry-Kravis, MD, PhD, profesora de pediatría, ciencias neurológicas y bioquímica en Rush Centro Médico de la Universidad. «Estoy emocionado de participar en un estudio doble ciego controlado con placebo de cannabidiol en Fragile X. Espero ser parte del esfuerzo para mover lo que puede ser el primer producto indicado específicamente para el síndrome X frágil hacia la disponibilidad para mis pacientes».
Zynerba anclará la escala CGI-I a los síntomas de comportamiento de las discusiones recientes basadas en FXS celebradas con la FDA,
También se recopilarán datos cualitativos adicionales sobre la relevancia clínica de otros comportamientos del SXF para cuidadores y pacientes a fin de mantener la coherencia con la orientación reciente proporcionada por la FDA sobre cómo reflejar de manera adecuada y precisa la voz del paciente durante el desarrollo del medicamento.
También se solicitará una reunión con la FDA para determinar la aceptabilidad de los datos del ensayo como base para la presentación de la Solicitud de Nuevo Medicamento (Drug Drug Administration, NDA) si se obtienen resultados positivos del ensayo. Los resultados principales se esperan para la segunda mitad de 2019.
Artículos relacionados: síndrome de X frágil, enfermedades raras, investigación
Fuente: https://goo.gl/v8vaVk