Canadá:
Según una historia de pm360online.com, la compañía de biotecnología global Shire plc anunció recientemente que su producto Takhzyro (lanadelumab inyectable) fue aprobado por Health Canada luego de una revisión prioritaria. Takhzyro está indicado como un tratamiento periódico y de rutina para los ataques de hinchazón que ocurren con la rara enfermedad hereditaria de angioedema. El medicamento está aprobado para pacientes de 12 años o más.
Sobre el angioedema hereditario
El angioedema hereditario es un trastorno genético que se caracteriza por episodios crónicos de inflamación que pueden afectar varias áreas del cuerpo. La condición es causada por mutaciones que afectan el gen HAE. Los ataques de hinchazón generalmente ocurren aproximadamente cada dos semanas; Por lo general, pueden durar varios días. La hinchazón puede afectar las extremidades, el tracto digestivo, la cara y las vías respiratorias, y la obstrucción de las vías respiratorias es la complicación más peligrosa. El vómito y el dolor abdominal pueden acompañar el ataque también si el tracto digestivo está involucrado. El tratamiento implica reducir la probabilidad de aparición de ataques y evitar que empeoren cuando lo hacen. El angioedema hereditario suele ser solo mortal si no se trata. Se estima que la prevalencia de la afección es de alrededor de uno en 10,000 a uno en 50,000, al menos en los Estados Unidos y Canadá.
Acerca de Takhzyro
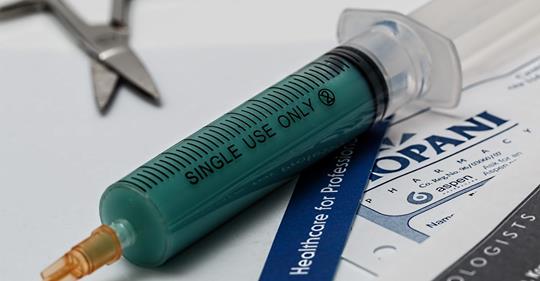
Takhzyro generalmente se dosifica a intervalos de dos semanas, similar a la frecuencia promedio de ataques de angioedema hereditario. Sin embargo, si los pacientes parecen estar respondiendo bien durante un período de seis meses, esta dosis se puede volver a marcar aproximadamente una vez al mes. El fármaco ha funcionado de manera impresionante en los ensayos; en intervalos de dos semanas, fue capaz de reducir la cantidad de ataques de hinchazón por mes en un 87 por ciento, y en intervalos de cuatro semanas, podría reducir la cantidad en un 73 por ciento. Los efectos secundarios también son relativamente leves y se limitan a las reacciones en el lugar de la inyección. La inyección también puede ser autoadministrada.
La aprobación de Takhzyro por Health Canada sigue relativamente de cerca la aprobación del medicamento en los EE. UU., Que se aprobó por primera vez el 23 de agosto para la misma indicación. Debe tenerse en cuenta que este medicamento está destinado a la prevención de ataques y no está destinado a reducir un episodio de inflamación que ya ha comenzado.
Artículos relacionados: angioedema hereditario, trastorno genético, ensayos clínicos
Fuente: https://goo.gl/wrMv95